自然免疫システムと遠隔転移の関係を究明し、人々が安心してがん治療に向き合える未来へ「がんの遠隔転移は予防できるのか?」
医学部附属病院 放射線部 助教
中島 良太
高等研究院 物質-細胞統合システム拠点(iCeMS) 教授
鈴木 淳

京都大学創立125周年記念事業の一つとして設立された学内ファンド*「くすのき・125」。このファンドは、既存の価値観にとらわれない自由な発想で、次の125年に向けて「調和した地球社会のビジョン」を自ら描き、その実現に向けて独創的な研究に挑戦する次世代の研究者を3年間支援するというものだ。
*「学内ファンド」とは、京都大学がめざす目標に向けて、京都大学が持つ資金を学内の教職員等に提供する制度のことです。
2020年度に採択されたiCeMSの鈴木淳先生の研究テーマは、「不要細胞の除去から目指す健康寿命の永続」。鈴木先生は、死んだ細胞や生きた細胞の不要な部分を除去するという、ヒトに備わった機能について研究を進めている。この機能を解き明かすことが、病気になることを未然に防ぐ先行医療につながるのだという。鈴木先生の挑戦について、動画メッセージとインタビューで伺った。
鈴木先生の研究テーマについて教えてください。
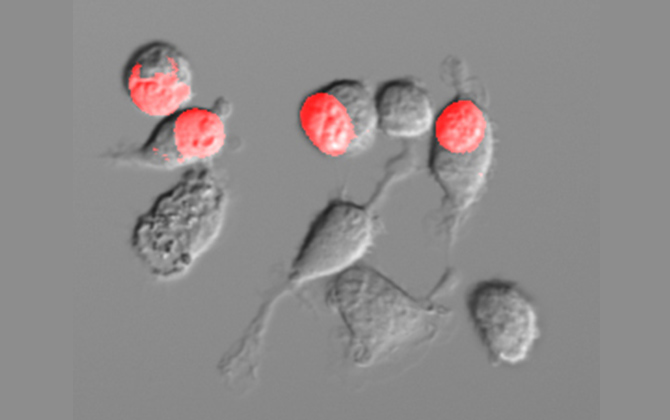
「私たちの身体のなかでは、毎日100-1000億個ほどの細胞が、役目を終えて死んでいきます。私は、この死んだ細胞が除去されるメカニズムについて研究しています。死ぬ間際の細胞は『私を食べて』というシグナルを出し、それを感知した白血球の一種、マクロファージに食べられるのですが、実は細胞が食べられることは私たちの健康にとってとても重要なことなのです。たとえば、死んだ細胞が破裂して内容物が放出されると免疫細胞が過剰に反応して炎症が起きてしまいます。食べられることで内容物が外に出ず炎症を防ぐことにつながるんですね。私は、死んだ細胞が食べられる仕組みを解明し、病気の予防につなげようという研究をしています」
どのようなきっかけでこの分野に興味を持たれたのでしょうか。
「大学院では細胞のがん化機構に関する研究をしていたのですが、私がやっていたがん研究の領域は、当時、欧米を中心にかなり多くの研究者が参入していました。そのため研究といっても他人の論文を読んで仮説を立てて進めることが多く、どこか他人の土俵で相撲を取っているような歯がゆさを感じていたんです。もっと一から自分で新しい分野を打ち立てるようなことがしたい、そう考えて、ポスドクをはじめる際に細胞死というテーマに方向転換したんです。
細胞が死ぬ細胞死という現象そのものについては、2002年にノーベル賞受賞者が出るなど注目されてはいましたが、実際のメカニズムはわかっていないことばかりです。死んだ細胞が食べられる仕組みもその一つ。細胞が死ぬと、細胞の内と外が裏返って細胞内にあるホスファチジルセリン(PS)という脂質が表に出てくるのですが、このPSの露出を検知することで、マクロファージが細胞の死を感知するということは、1980年代にはわかっていました。そこから、この現象は何かしら特定のタンパク質によって引き起こされるのではないか、という仮説が立てられてきましたが、20年ほど経っても謎のままでした。そこで、私は死んだ細胞が食べられる仕組みを解明したいと考え、この分野で素晴らしい仕事をされていた京都大学大学院医学研究科の長田重一教授の研究室に入らせてもらうことにしました」

あえて新しいことに飛び込むのも、自分で切り開いていこうとするのも、相当な覚悟が必要だったのではないでしょうか。
「私が選んだ、PSの露出に関わる分子を特定するというテーマについては、長田先生も難しいとおっしゃいました。ただ当時の私は博士号を取ったばかりのポスドクで、何も背負うものはなく、研究だけに没頭できる環境にいたんです。結果を出さないと研究を続けていくのは難しくなるという厳しさも十分わかってはいましたが、リスクをとってチャレンジできるのは今しかないと思ったのです。とはいえ、実際にはじめてみると、やはりかなり手ごわいテーマでした。1年ぐらいは思うようなデータが取れず、論文を書くような状況ではありませんでした。プロの研究者としては最悪の状態です。その頃に結婚して新婚旅行に出かけましたが、ふと実験のうまくいかないことがよぎってしまう(笑)」
どのようなところが手ごわかったのでしょうか。それを、どのようにして乗り越えられたのかについてもお聞かせください。
「細胞が死ぬ時に何が起こっているのかを調べること自体が、とても難しかったんです。当然ですが、細胞が死んでしまうと、それ以上細胞を増殖させることはできませんよね。でも増殖させないことには、そこにどんな分子が関わっているのかという情報を得ることができないのです。もがき続ける中であるとき、本来は細胞が死ぬ時に出るPSを、生きた細胞が出せるようにできないかということに思い至りました。生きた細胞がPSを出すのなら、その細胞を増殖させて調べることができるというわけです。
しかし、このアイデアが生まれてからも1年ぐらいは試行錯誤が続きました。アプローチを変えては実験で試してみるのですが、思ったような結果が出ないのです。ただ、長田先生と一緒に研究したおかげで、一つひとつの実験を最後までやり通す姿勢が身につきました。一つの実験をしっかり終わらせることで、たとえ失敗に終わってもそのアプローチをたくさんの選択肢のなかから除外することができる。地道に実験を重ねる中で、少しずつですが前進することができました。そしてついに、細胞が生きている間にPSを出せる条件を見つけ出すことができました。この条件をもとに、さらに多くの研究を重ね、2010年、2013年と私たちのグループはPSを露出させる2種類のタンパク質を世界で初めて発見することに成功しました」
大きな成果ですね。その後も、死んだ細胞を除去するメカニズムの解明を続けてこられたのですか?
「はい、さまざまなアプローチを行っています。2017年に京都大学iCeMSに移ってからは、PSを露出させるタンパク質がどのように活性化するのかを、テーマの一つに据えました。このタンパク質を働かせるために何か別の因子が関わっていることが想定されており、それを突き止めようと考えたのです。以前のように生きた細胞にPSを出させるのではなく、本来のメカニズムである、細胞が死にゆく過程からでもうまく情報を抽出できる新しい技術を開発し、2021年、活性化に関わる因子を明らかにすることができました。
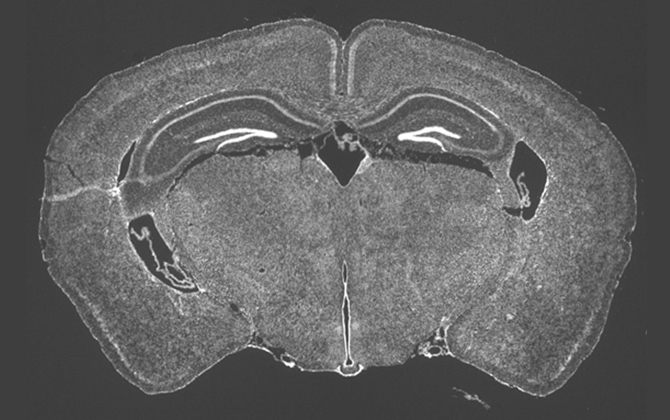
また、これまでは『死んだ細胞』を除去する仕組みの解明に注力していましたが、今は、『生きた細胞』が持つ不要な領域を除去する仕組みについても探っています。特に着目しているのは、脳の神経細胞です。脳の神経細胞は一度作られたら消滅することはなく、老化して傷んでしまった部分を除去し、そこだけ新しいものに作り替えたりしながら一生使い続けられます。脳の神経細胞において不要なものが除去されていく仕組みはまだわかっていませんが、どうやらPSが関わっていることは間違いなさそうです。これまでの研究成果を基盤にしながら、その仕組みに迫れるのではないかと思っています」
「くすのき・125」では、応募の際に「125年後の調和した地球社会のビジョン」をお聞きしています。鈴木先生はどのような社会をめざしていらっしゃるのでしょうか。
「万人が健康に過ごせる社会です。人生100年時代と言われ健康寿命の重要性が叫ばれていますが、今の医療は対症療法が中心で症状が出てから治療するため、気づいたときには病気がすごく進行していることもあります。このアプローチを根本から変え、症状が出る前から異常を検知し、修復することができれば、健康な状態をもっと維持できるようになると考えています」
先生の研究テーマ「不要細胞の除去から目指す健康寿命の永続」では、健康な状態の維持に対して、どのようにアプローチされるのでしょうか。
「研究のキーワードとしているのは、『リノベーション』です。建物のリノベーションと同じように、生体内では、老化や機能低下などによって異常を起こし不要になった細胞の全体や一部を除去し、新しいものを作って修復することが常に行われています。このリノベーションの働きが老化などによって衰えることで、様々な病気につながると考えられます。私は、まず細胞における正常なリノベーションの仕組みを解明したうえで、そのシステムがどのように働かなくなっていくのかを突き止めたいと思います。さらに、システムがうまく機能するように外から手助けできるところにまで到達したいというのが、私の研究の目標です」

リノベーション機能の働きが衰えることで、どのような病気が起きるのでしょうか。
「たとえば、脳の神経細胞では、不要なタンパク質が除去されないと、アルツハイマーや小脳変性失調症などの神経変性疾患が起こることがわかっています。不要なタンパク質が除去されずにたまることで、正常な細胞が死んでしまうのです。それなら、不要になっても除去されないというリノベーション機能の低下がはじまったごく初期の段階で異常をつかみ、食い止めることができれば病気になること自体を防げるかもしれません。別の例としては、不要な細胞を攻撃して除去しようとする免疫細胞の働きもリノベーションと捉えることができます。がんが進行する過程でリノベーションの働きが、がんによって弱められてしまうということが起こります。免疫細胞の働きを薬などによって強め正常に働くようにするのが免疫療法ですが、もし免疫細胞によるリノベーション機能が低下しはじめた初期の段階で異常を検知できれば、がんも悪性化する前に治療できるかもしれません。放っておくと病気になるかもしれない異常を芽のうちに摘んでしまおうという先行医療です」
「くすのき・125」の支援を受ける3年間で、具体的にはどんな取り組みを進めたいと考えていますか。
「大きく分けると二つあります。一つは、不要な細胞が除去される仕組みの解明と応用です。不要な細胞の中でも死んだ細胞の除去に関してはある程度わかってきましたので、その成果を活用して、老化した細胞、機能の落ちた細胞についても認識され、除去される仕組みを突き止めたいと思っています。そこで明らかになったことを応用すれば、健康寿命を延ばすことに直接的に貢献できるはずです。たとえば、細胞がダメになっているという情報をとらえられるマーカーのようなものを見つけるというのも、その一つです。このマーカーを使って、血液検査やさらにもっと身体への負担の少ない方法で調べられるようになればいいですよね。
細胞の異常を検知できるようになれば、もう一歩進めて、除去する方法の開発にも挑戦していきたいです。投薬することで、細胞を殺してマクロファージにがん細胞を食べるように仕向ける抗がん剤は既にあります。でも、この抗がん剤を使うとマクロファージがすごく弱るんです。私たちは薬を使わずにマクロファージに不要なものを認識させ、食べさせて除去するという方向で、治療法の開発を進めていくつもりです。
もう一つは、生きた神経細胞の不要な領域が除去される仕組みの解明です。こちらのテーマについては、基本的な仕組みがまだよくわかっていないのでその解明から進めていきます。どうやらPSを露出させるには複数の仕組みがあり、それらを使い分けて不要な領域ごとに除去しているようですが、どのように領域を決めているのか、神経細胞にもいろいろな種類がある中で何をどう使い分けて除去しているのかなど、理解しなければならないことはたくさんあります。臨床までの道のりは遠いのですが、原理や背景にあるものを理解したうえでないと、本当に有効な応用技術は生まれないと思っています」
高等研究院 物質-細胞統合システム拠点(iCeMS) 教授
医学博士(大阪大学)。大阪大学大学院医学研究科博士課程修了。京都大学大学院医学研究科 助教、大阪大学免疫学フロンティア研究センター寄付部門准教授を経て、2017年1月より現職。専門は医生化学、細胞膜生物学。2014年科学技術分野の文部科学大臣表彰若手科学者賞、日本生化学会奨励賞受賞。2021年3月、論文“Caspase cleavage releases a nuclear protein fragment that stimulates phospholipid scrambling at the plasma membrane”(核内タンパク質の断片が細胞膜のリン脂質スクランブルを活性化する)が、米国科学雑誌モレキュラーセル誌(セルプレス)にオンライン公開。